Содержание
- 1 С чего начиналась хирургия рака молочной железы
- 2 Когда женщины стали выживать после операций по удалению рака молочной железы
- 3 Когда и как операции при раке молочной железы стали более щадящими
- 4 Как выглядят операции при раке молочной железы сегодня
- 5 Как будут выглядеть операции при раке молочной железы в будущем
История лечения самого распространённого рака среди женщин.
С чего начиналась хирургия рака молочной железы
Впервые оперативные попытки лечения рака молочной железы упоминаются в папирусе Эдвина Смита, или хирургическом папирусе. Он датируется 1600 годом до н. э. В нём описаны восемь случаев опухолей и язв молочной железы, которые были удалены прижиганием металлическим раскалённым инструментом. О болезни в тексте говорится так: «Лечения не существует».
В 5 веке до н. э. Гиппократ описал женщину с кровянистыми выделениями из соска и раком молочной железы и не рекомендовал хирургическое вмешательство. Он понимал, что операция только сократит жизнь заболевшей. Кстати, Гиппократ одним из первых применил термин carcinos и carcinoma.
В I веке нашей эры греческий врач Леонид лечил женщин по следующей технике: кожа груди разрезалась, а затем молочная железа прижигалась до тех пор, пока полностью не обугливалась и не отделялась от грудной стенки. После операции пациентки ухаживали за раной дома. Большая часть прооперированных таким образом женщин ожидаемо погибала от инфекций.
Из-за высокой смертности методика прижигания не получила большого распространения. Но сегодня способ Леонида известен как эшаротомия. Она используется для лечения последствий ожогов всей толщины кожи.
Врачи продолжали искать методы борьбы с раком молочной железы. Но в XIV–XVI веках обезболивающих препаратов по-прежнему не было, поэтому доктора старались тратить на операции как можно меньше времени. Одним из быстрых вариантов удаления молочной железы был гильотинный метод. Врач ампутировал молочную железу длинным острым ножом.
Есть свидетельства того времени, как хирург без предупреждения приходил в дом женщины, чтобы провести операцию. Помогали врачу в жестоком лечении несколько мужчин, которые удерживали пациентку на её кухонном столе. Швы после операции не накладывали, грудную клетку туго бинтовали для пережатия повреждённых сосудов. Неудивительно, что большая часть женщин после вмешательства умирала от кровотечений.
Но всё же были и те, кто переживал ранний послеоперационный период. Например, так было с Доньей Хосефой Перес Мальдонадо. Мексиканку прооперировали 25 апреля 1777 года. Врач удалил шесть опухолей из её груди. Донья заказала художнику задокументировать всё, как было, для написания картины в дар святому за исцеление от недуга. Женщина прожила пять месяцев после операции.

Интересно, что в это же время жестоких операций появился хирург, предложивший сохранять кожу и сосок, не поражённые опухолью. Доктор Жан Луи Пети, по сути, создал прообраз современной кожесохраняющей мастэктомии. Однако, учитывая более распространённые представления того времени об оптимальном лечении опухолей, Пети был принят за еретика.
Когда женщины стали выживать после операций по удалению рака молочной железы
Уильям Стюарт Холстед был одним из лучших выпускников медицинского факультета Колледжа врачей и хирургов Колумбийского университета 1877 года. Врач начал практиковать, когда хирурги оперировали без перчаток, халатов, масок и шапочек, лишь закатав рукава. Инструменты и руки мыли периодически, не для профилактики раневой инфекции. Операции проводили быстро, потому что возможности обезболить пациента пока не было.
Поначалу американский хирург воспринимался коллегами с усмешкой. Присутствовавшие на его операциях подшучивали над ним и говорили, что до Холстеда не видели, чтобы часть раны успевала затянуться уже во время операции — так долго, аккуратно и тщательно по сравнению с современниками он мог работать.
Для лечения рака молочной железы Уильям Стюарт предложил операцию, которая и сегодня носит его имя — мастэктомия по Холстеду. Методика была основана на выводах из наблюдений за пациентками, страдающими раком молочной железы. Они показывали: у женщин с метастатическим поражением лимфатических узлов более высокий риск умереть от прогрессирования рака молочной железы, чем у пациенток без метастазов в лимфатических узлах.
На основе наблюдений Холстед выдвинул центробежную теорию — опухоль появляется в молочной железе, затем распространяется в расположенные рядом лимфатические узлы, а потом в другие органы. От этого и умирают пациентки. Логичным в такой ситуации было «прервать путь» распространения метастазов и всем пациенткам. Особенно тем, у кого нет признаков поражённых лимфатических узлов, а также удалить заранее все рядом расположенные лимфатические узлы.
Центробежная теория способствовала дальнейшему росту агрессивности хирургического лечения. Ведь выяснилось, что также ближайшими и фильтрующими лимфу от молочной железы, то есть региональными для молочной железы являются парастернальные лимфатические узлы. Они находятся рядом с грудиной, внутри грудной полости. А если они региональные, значит, тоже могут быть источником отдалённых метастазов и должны быть удалены вместе с первичным очагом для профилактики рецидива.
Далее была разработана методика мастэктомии по Урбану — Холдину — Дымарскому, включившая в себя помимо объёма операции Холстеда ещё и резекцию 2–4 рёбер для удаления парастернальных лимфатических узлов.
Внедрение операции Холстеда снизило послеоперационную летальность, но такое лечение продолжало оставаться жестоким. Пациентки сталкивались с чудовищными осложнениями: значительным лимфатическим отёком, ограничением движений в плечевом суставе, деформации грудной стенки, выраженными болями.
Но нельзя не сказать, что сегодня хирургия имеет лицо, которое во многом создал Холстед. Благодаря ему появились тщательное мытьё рук, обработка инструментов и области оперативного вмешательства антисептическими растворами перед операцией, экономный разрез, контроль кровотечения.
Когда и как операции при раке молочной железы стали более щадящими
За пациентками после радикальных и сверхрадикальных вмешательств наблюдал не только Холстед. Всё больше женщин выживали после операций и сталкивались не с прогрессированием рака молочной железы, а с ужасающими последствиями операций. Учёный Бернард Фишер предложил посчитать, оправданно ли агрессивное хирургическое лечение при заболевании.
В 1970-х исследовательская группа NSABP во главе с Фишером подобрала дизайн исследования. В первом эксперименте пациенток распределили в группы:
- радикальной мастэктомии — удаление молочной железы, подмышечных лимфоузлов, большой и малой грудных мышц;
- ампутации молочной железы с облучением регионарных лимфатических узлов и мастэктомии;
- ампутации молочной железы без воздействия на регионарные лимфатические узлы.
Во втором эксперименте участниц распределили в группы радикальной мастэктомии и мастэктомии с облучением зон регионарного лимфооттока.
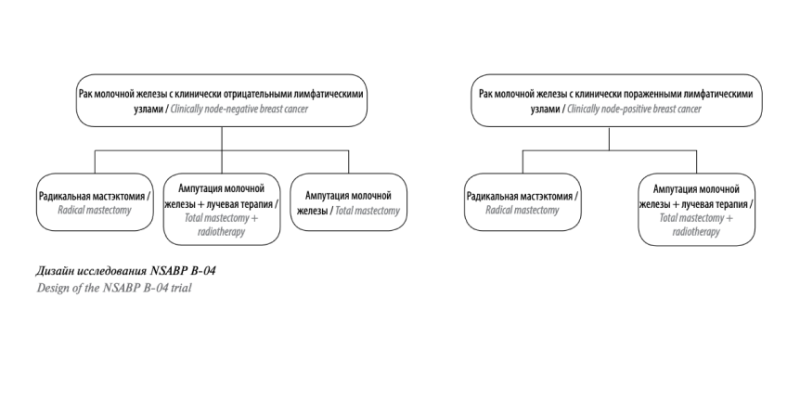
Исследование заняло 25 лет. Команда NSABP публиковала результаты наблюдения через 3, 5 и 10 лет, и каждый раз они были идентичными. Оказалось, что удаление здоровых тканей, окружающих опухоль, — лимфатических узлов, мышц — не помогает снизить риск прогрессирования заболевания.
Параллельно с новым представлением об онкологии стали появляться другие методы лечения: радиотерапия и химиотерапия, гормонотерапия.
Последние десятилетия активно изучаются другие препараты — для таргетной терапии и иммунотерапии. Лекарственное лечение сначала назначалось после операции для снижения риска рецидива и показало эффективность. Позже врачи стали назначать препараты перед операцией, чтобы последняя стала возможна. Так, многих пациенток смогли прооперировать с меньшим количеством осложнений и с лучшими результатами.
Сегодня для некоторых видов рака молочной железы предоперационная терапия стала стандартом помощи даже при небольших размерах опухоли и отсутствии поражения лимфатических узлов. Такой подход связан с тем, что опухоль, подвергшуюся предоперационной терапии, можно удалить и исследовать на признаки, которые подскажут, что лучше назначить после операции. А иногда опухоль и вовсе исчезает после лекарственного лечения.
Всё это дало основу для уменьшения объёма операций при раке молочной железы без увеличения риска рецидива заболевания.
Как выглядят операции при раке молочной железы сегодня
За последние 50 лет характер операций при раке молочной железы значительно изменился. Учитывая результаты исследований группы NSABP и других, объём вмешательства становился меньше и избирательнее. Процедура трансформировалась от радикальной мастэктомии с удалением мышц к удалению молочной железы с сохранением мышц, а позже к частичному сохранению молочной железы или её кожи и соска с одномоментной реконструкцией.
Эти изменения привели нас в точку, где мы находимся сегодня: хирургия рака молочной железы не страшная, не карательная, а бережная и сберегательная, эстетическая.
Онкопластические техники — использование принципов пластической хирургии для восполнения дефектов после удаления опухоли позволяют улучшить вид молочной железы после лечения. Мы сегодня не представляем операции на молочной железе без возможности одномоментной и в некоторых случаях отсроченной реконструкции.
Нормальная практика — обсуждать с пациенткой возможные варианты хирургического лечения, которых практически всегда несколько. В каждом случае учитываются ожидаемые эстетические и функциональные риски. А онкологические риски во всех вариантах хирургического объёма равны и при полном удалении опухоли, и при проведении лучевой терапии, если орган сохраняют.
Сейчас продолжают находиться клиники и хирурги, выполняющие операцию Холстеда в классическом варианте при раннем раке молочной железы. Но всё-таки теперь мы понимаем, что на это нет никаких оснований.
Как будут выглядеть операции при раке молочной железы в будущем
Мы вплотную подошли к возможности удаления ложа опухоли только с помощью вакуумной системы после успешной предоперационной химиотерапии.
Только представьте, каким можно увидеть будущих пациенток, столкнувшихся с раком молочной железы через 5–10 лет. Женщина приходит на процедуру из дома, потому что нет смысла её госпитализировать. Она не голодает, как обычно это требуется перед вмешательствами по типу мастэктомии или частичного удаления молочной железы. Место, в котором определялась опухоль, можно будет убрать под местной анестезией с помощью специального аппарата, который под отрицательным давлением соберёт весь биологический материал и через который можно провести манипулятор для остановки кровотечения, если это потребуется. Контролировать подобную операцию можно будет ультразвуковым датчиком. И самое важное: через 2–3 часа после процедуры пациентка сможет заниматься привычными делами. Например, ехать на работу, домой или пойти на прогулку. А реабилитация такая же, как после удаления доброкачественной опухоли из молочной железы, например фиброаденомы.
Пока это не стандарт лечения, мы в процессе сбора данных, но такой объём операции наверняка совсем скоро будет внедряться в ежедневную клиническую практику.

